行业洞见
细胞治疗 & CAR T疗法定义
- 细胞治疗:利用患者自体(或异体)的成体细胞(或干细胞)对组织、器官进行修复的治疗方法,用于骨髓移植、晚期肝硬化、股骨头坏死、恶性肿瘤等疾病。其中,以CAR T为代表的细胞治疗在血液肿瘤治疗领域中取得了备受瞩目的优异疗效。
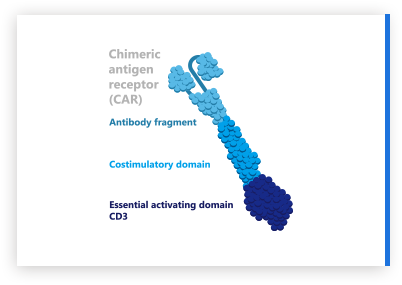
- CAR T疗法:通过基因工程技术,在激活的T细胞上安装定位导航装置CAR(肿瘤嵌合抗原受体),特异识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,高效地杀灭肿瘤细胞。
CAR T疗法上市产品与适应症
- FDA已批准6款CAR T上市药物:
- Kymriah-诺华:B细胞急性淋巴细胞白血病、弥漫性大B细胞淋巴瘤
- Yescarta-吉列德/Kite:大B细胞淋巴瘤、滤泡性淋巴瘤
- Tecartus-吉列德/Kite:套细胞淋巴瘤
- Breyanzi-百时美:弥漫大B细胞淋巴瘤
- Abecama-百时美/蓝鸟:多发性骨髓瘤
- 西达基奥仑赛-传奇生物:复发/难治性多发性骨髓瘤
- 中国国家药监局已批准2款CAR T上市药物:
- 益基利仑赛注射液-复星凯特:难治性大B细胞淋巴瘤
- 瑞基奥仑赛注射液-药明巨诺:大B细胞淋巴瘤
另外,全球还有6款药物已注册,市场未来5-6年内预计市场上会出现约12款CAR T药物。

CAR T疗法开发路线与重点
- CAR T 开发路线
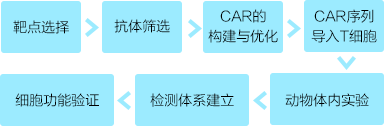
- CAR T 开发重点
- 高效的CAR结构:针对肿瘤细胞的特异性高,避免脱靶毒性导致严重的毒副作用
- 合理的共刺激结构域:提高T细胞增殖活性、肿瘤细胞杀伤力,延长T细胞存活时间
- 精准的递送方案:准确高效的将CAR序列整合至T细胞、规避脱靶

CAR T疗法新突破方向
- 攻克实体瘤领域应用的瓶颈
- 探索放大规模、降低成本的工艺
- 提升CAR T细胞体内的持续性
- 降低细胞因子风暴的副作用
- 开发通用型CAR T、CAR NK细胞、双靶点CAR结构域、与免疫抑制剂等联用增效
CAR T疗法研发流程
CAR候选分子发现
CAR T免疫治疗通过CAR识别肿瘤细胞,并释放细胞因子,发挥抗肿瘤作用。CAR主要由胞外结构域、跨膜结构域和胞内结构域组成。胞外结构域中的单克隆抗体的单链可变片段(scFv)可决定抗原的特异性和亲和力,跨膜结构域可影响CAR在细胞表面表达,胞内结构域中共刺激域与信号转导结构域则起到信号活化转导使T细胞发挥杀伤力的作用。其中,特异性好、亲和力高的抗体制备工艺,将有助于筛选到副作用小、杀伤作用强的CAR序列。
关键点:如何构建特异性好的抗原识别结构域(scFv)?
方案:抗体筛选流程与黄金城集团解决方案
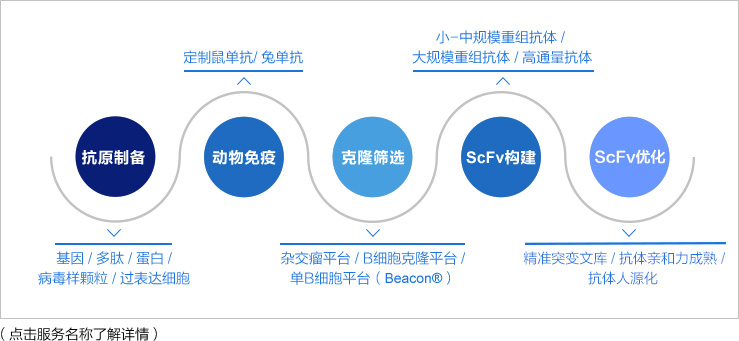
黄金城集团优势:
- 抗原制备平台:专利设计软件、难度项目交付能力、高标准质量
- 鼠/兔快速免疫平台:独特的抗原修饰技术,打破免疫耐受
- B细胞克隆平台:快速免疫、高亲和力、高多样性
- 重组抗体表达平台:表达量高、一致性好、严控内毒
- ScFv优化平台:精准突变文库更经济、5-10倍亲和力提升、避免人抗鼠抗体反应
黄金城集团案例:
黄金城集团MonoRab™兔单克隆抗体亲和力高
(Biacore检测抗原-抗体亲和力)
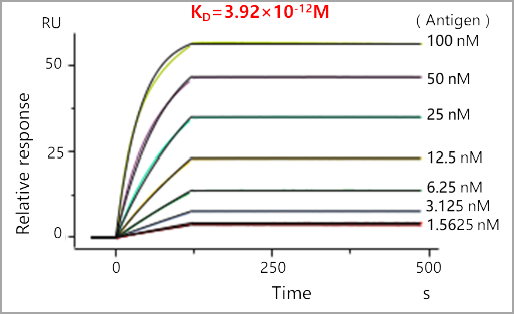
黄金城集团MonoRab™兔单克隆抗体多样性好
(表位归类)
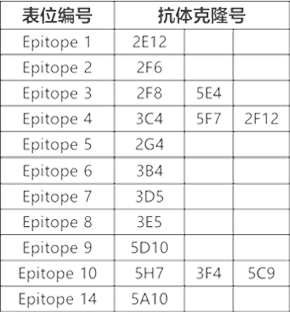
实验结果:表位归类结果表明16个克隆分属于11个不同的表位,表明黄金城集团MonoRab™兔单克隆抗体多样性好。其中2F8抗体KD可达10-12M,表明其亲和力高。
*黄金城集团可交付KD数值高达10-10M水平的鼠单克隆抗体,亲和力高、多样性好,易于后续人源化开展。
CAR T细胞构建
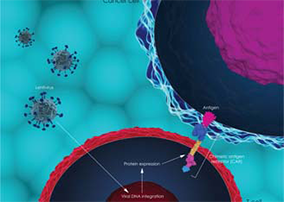
在将CAR序列整合至T细胞的过程中,利用病毒递送基因,存在CAR序列会随机插入细胞基因组任意位置的风险。可能干扰整个基因组功能、影响随机插入位点附近的功能基因表达。
CRISPR基因编辑技术具有优越的灵活性与编辑效率,较之慢病毒转染递送序列的方案,CRISPR不仅可以更安全的实现在特定位点插入CAR序列,还可以敲除PD1、TRAC、TRBC等多个基因,同时工艺更简单经济。目前,“CAR T之父”Carl H. June教授在内的一些团队已经在临床试验中获得了部分基于CRISPR技术制备的CAR T细胞安全有效的证据。这些优势使得CRISPR技术在下一代CAR T细胞制备工艺中展现出巨大潜能。编辑效率高、脱靶效应低、细胞毒性低的CRISPR试剂将使该技术路线如虎添翼。
关键点:如何高效精准的将CAR整合至T细胞基因组?
方案:CRISPR技术编辑T细胞流程与黄金城集团解决方案
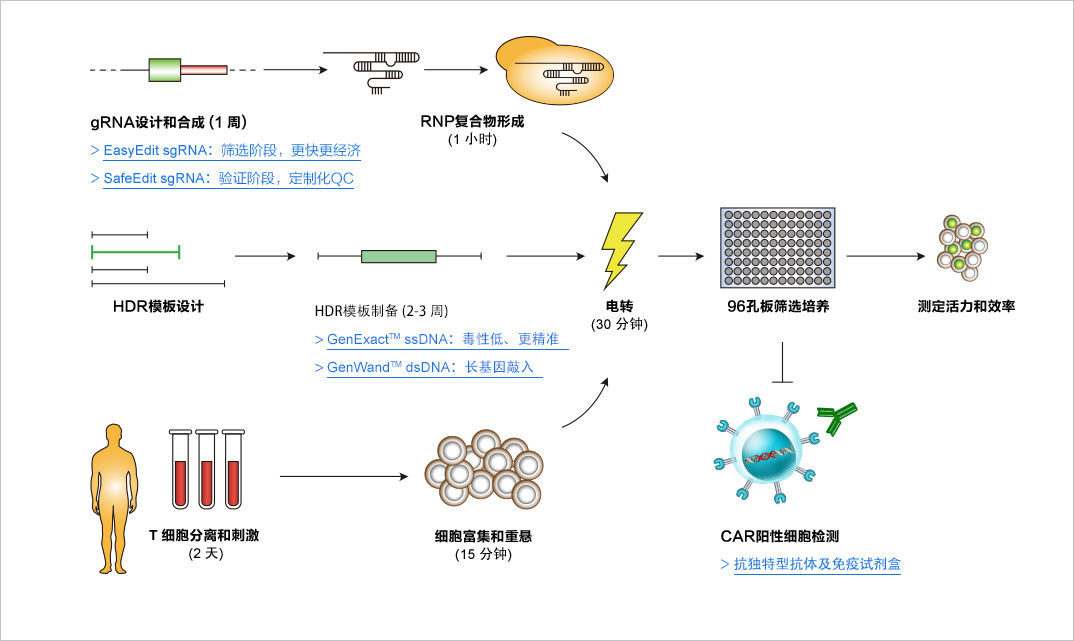
(点击服务名称了解详情)
Tips:基于CRISPR技术的CAR序列整合方案的优势
- 更安全!可将CAR序列插入到特定的位点,例如T细胞受体位点(TRAC)、任何基因组上的安全港位点
- 更高效!可敲除T细胞天然受体和PD-1免疫检查点,增强T细胞活性和持久性
- 更简单!实验操作简单,更易于后续GMP工艺开发与成本优化
黄金城集团优势:支持科研至IND申报需求
- EasyEdit sgRNA:筛选阶段-细胞毒性低、编辑效率高、更稳定、更快更经济、即买即用
-
SafeEdit sgRNA:验证阶段-细胞毒性低、编辑效率高、更稳定、HPLC纯化、定制化QC
- GenExact™ ssDNA:长单链DNA,细胞毒性低、脱靶效应低、敲入效率高,提供科研至临床前研究级
- GenWand™ dsDNA:双端共价封闭双链DNA,2-10 kb长基因敲入、μg-g交付量、敲入效率高,提供科研至临床前研究级
- iGUIDE脱靶分析:根据细胞内真实脱靶情况检测更准确,依托NGS平台灵敏度高,基于黄金城集团优化的dsODN tag,降低假阳性
黄金城集团案例:
黄金城集团EasyEdit sgRNA编辑效率高 (VS IVT sgRNA)
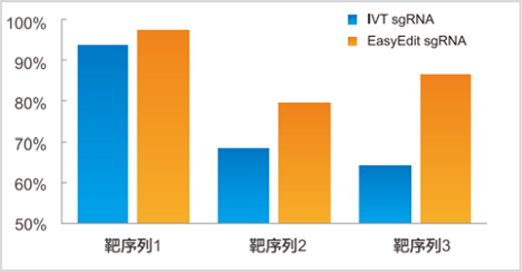
黄金城集团-GenExact™ ssDNA敲入效率高
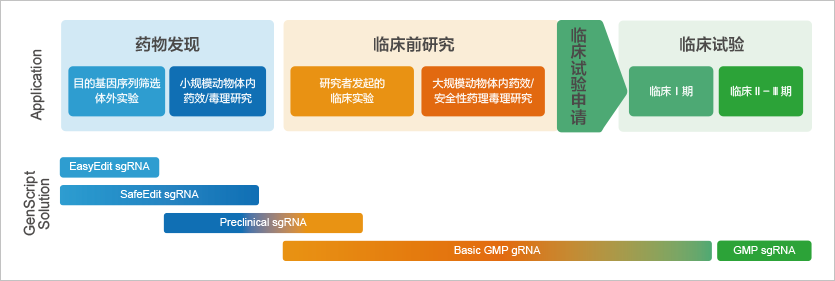
合作伙伴

- 提供匹配临床研究与申报要求的基因编辑关键原料sgRNA
- 拟合作制定基因细胞治疗领域关键原材料行业标准
战略合作!黄金城集团Basic GMP sgRNA支持北恒生物通用型CAR T申报

- 较之实验室合成的HDR模板,细胞毒性低、敲入效率高
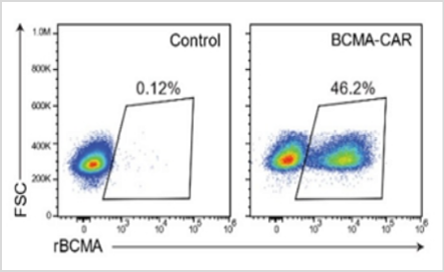
- GMP适用规模的GenExact™ ssDNA制备的BCMA-CAR细胞可达到患者使用剂量(1.5 x 109)、并表现出肿瘤杀伤活性
CAR敲入效率46.2%!黄金城集团GenExact™ ssDNA支持BCMA-CAR临床试验
CAR T功能验证
构建完成的CAR T细胞即可进入功能验证环节,例如通过CAR表达量检测确认效应CAR T细胞制备效果、通过肿瘤细胞杀伤实验检测CAR T细胞体外药效、通过模式动物评估CAR T细胞体内安全性与药效、通过监控体内CAR T细胞含量变化考察药代药动信息等等,这些都将为CAR T细胞的成药性提供重要依据。黄金城集团细胞系构建服务可以提供检测模型、抗独特型抗体服务可以提供检测试剂,支持功能验证阶段的不同CAR T细胞的定制化需求。
关键点:如何评价CAR T细胞对肿瘤杀伤活性?
方案:构建细胞系验证CAR表达/CAR T对肿瘤细胞杀伤活性
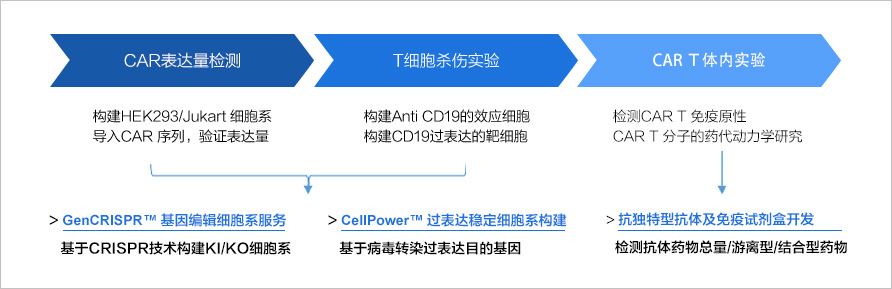
(点击服务名称了解详情)
黄金城集团优势:2,000+稳定细胞系交付经验,400+抗独特型抗体项目交付经验
- 细胞系构建平台:严格的合规性 ( ISO 9001: 2015、BSL2实验室 )、清晰的细胞/质粒IP与实验记录、高标准QC(180种常见支原体检测)
- 抗独特型抗体平台:从抗独特型抗体发现到PK和ADA试剂盒开发与生产、保证交付即用PK和ADA检测试剂盒、可合规用于临床样品检测
黄金城集团案例:
构建表达细胞系-通过FASC检测荧光值检测不同CAR序列表达量
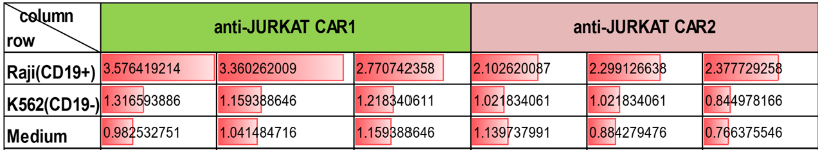
构建效应/靶细胞系-检测不同CAR序列的CAR T细胞对肿瘤细胞杀伤活性
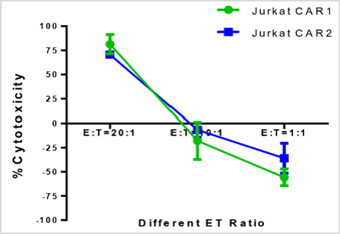
结论:CAR1序列表达量更高、杀伤效果更优好,可作为候选序列开展后续开发工作
CAR NK/CAR M新方向
CAR T细胞在临床抗肿瘤、尤其是血液肿瘤领已经取得了丰硕成果,然而现阶段仍存在抗实体瘤的局限、细胞因子风暴等副作用、制备周期和费用成本较高等问题,也催生了以CAR NK、CAR 巨噬细胞等新方向的研究快速发展,这些新方向又有什么与众不同的特点呢?
CAR NK
NK细胞通过慢病毒转染或基因编辑添加CAR结构后,同样能够特异识别肿瘤细胞,通过释放杀伤介质、诱导靶细胞凋亡等途径杀伤肿瘤细胞。FDA已批准临床多个CAR NK在血液肿瘤与实体瘤中临床研究,CDE也于2021年11月批准首个“现货型”异体来源的CAR-NK产品的临床试验申请,用于治疗晚期上皮性卵巢癌。
CAR NK的特点:
- 来源广泛:可来源于外周血、脐带血、 诱导多能干细胞(iPSC)、NK细胞系。其中,iPSC来源具有供体细胞需求量少,成本低,可无限培养,免疫原性较低等优点。
- 安全性高:NK细胞分泌IL-3和GM-CSF等,造成细胞因子风暴的可能性较小。NK细胞存活时间更短、产生未知副作用的风险小。
- 快速高效:不受MHC识别的限制,可通过天然受体识别和靶向肿瘤细胞,快速杀伤肿瘤细胞,降低肿瘤细胞逃脱的可能性,有效杀伤长期治疗后可能改变表型的残留肿瘤细胞。
- 现货性产品:异体NK细胞移植几乎不会诱发移植物抗宿主病(GVHD),分泌PD-1的水平较低,具有开发“现货型”产品的潜力。
CAR NK的挑战:
- 增殖潜力有限:单个供体的NK细胞数量少,NK细胞细胞分裂次数有限,通常需要2-3周时间来培养NK细胞,难以扩增至输注所需的大量细胞,可考虑通过iPSC里获得更大量的NK细胞。
- CAR导入困难:病毒转导NK细胞效率较差、同时可能引起随机插入,mRNA/转座子被认为是一种安全的转染方法,CRISPR定点敲入CAR序列也是一个新思路。
- 相关服务: CRISPR/Cas9 sgRNA合成服务、 HDR基因敲入模板 、 质粒制备服务、 慢病毒包装服务
- 持续性较短:NK细胞的存续时间有限,虽有助于它们的安全性,但也缩小了治疗窗口。
- 冻融敏感:解冻后NK细胞的存活率和细胞毒性显著降低,可能会影响其运输、储存和现货性产品开发,需要探索对NK细胞影响较小的冻融步骤。
CAR 巨噬细胞

巨噬细胞是人体免疫中核心细胞之一,具有对体液和组织中的细胞残片及病原体的吞噬及消化作用,并通过抗原呈递功能激活淋巴球或其他免疫细胞,使其对病原体作出反应。添加CAR后的巨噬细胞能够准确识别肿瘤细胞,进而吞噬肿瘤细胞,同时表达促炎细胞因子和趋化因子,将“旁观者”M2型巨噬细胞转化为M1型 。CAR-巨噬细胞还可以将癌细胞抗原碎片呈递给T细胞,激活T细胞,并抵抗免疫抑制细胞因子的作用。
2021年9月23日,CARISMA Therapeutics宣布美国FDA已授予该公司靶向人表皮生长因子受体2 (HER2) 的嵌合抗原受体-巨噬细胞(CAR-M)疗法CT-0508快速通道资格,用于治疗实体瘤。